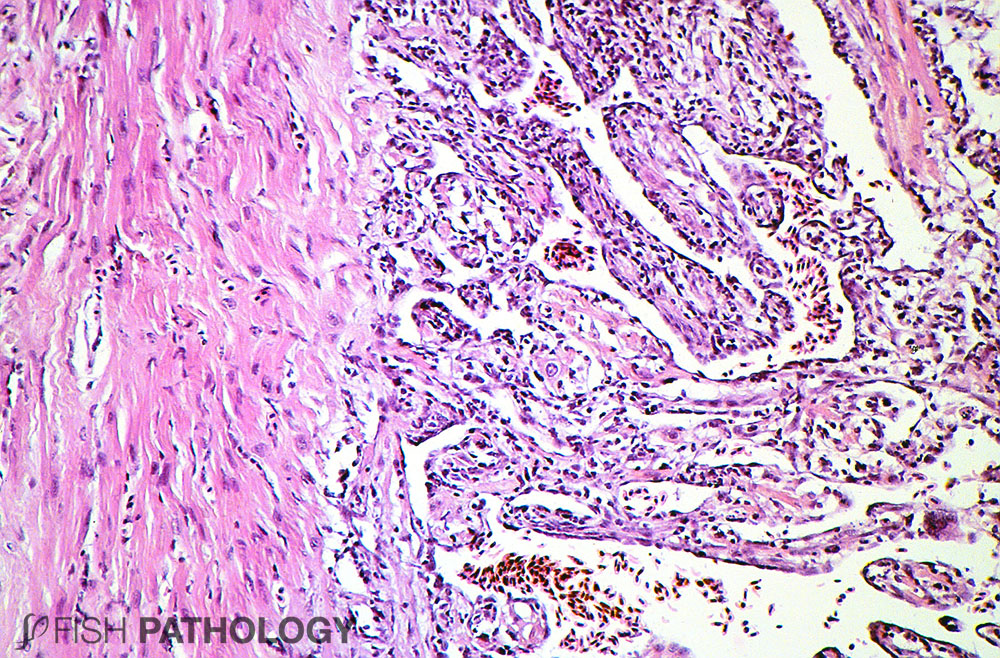
El Síndrome cardiomiopático (CMS) es una severa patología cardíaca que afecta al Salmón del Atlántico caracterizada por periodos prolongados de mortalidades generalmente bajas.

La enfermedad fue por primera vez reconocida en Noruega en 1985 en salmón Atlántico de cultivo y posteriormente en Islas Faroe, Escocia e Irlanda. CMS es una enfermedad trasmisible que se ha relacionado causalmente con Piscine Myocarditis Virus (PMCV), estrechamente relacionado con la familia Totiviridae.

CMS generalmente causa mortalidad en peces adultos o maduros después de 12 a 18 meses post transferencia al mar, causando pérdidas económicas sustanciales.
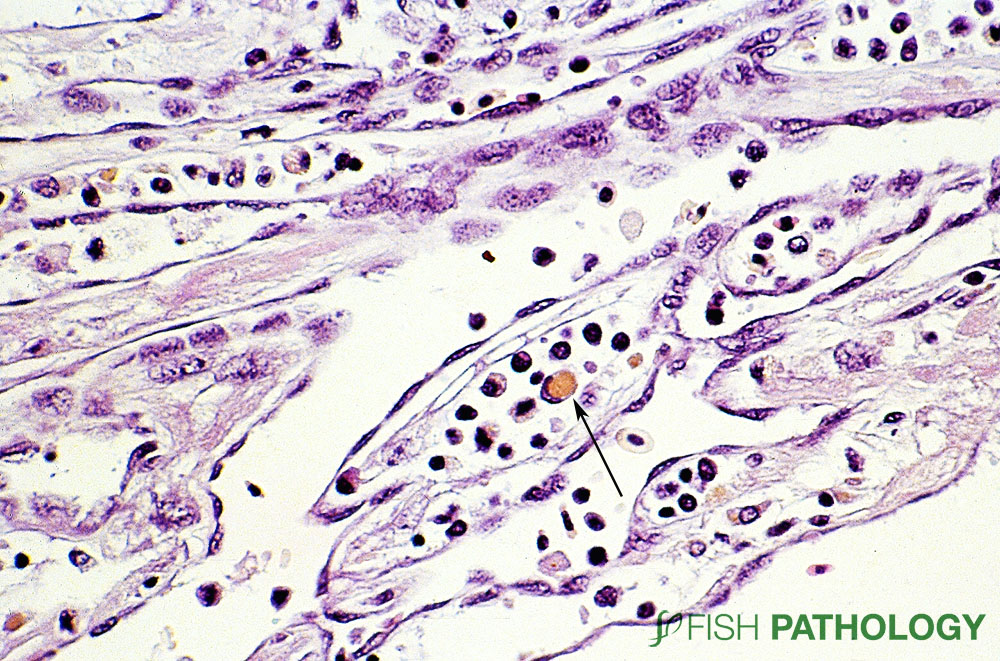
Las lesiones del Síndrome cardiomiopático comienza con inflamación de células endocárdicas e influjo de células inflamatorias en el miocardio, acompañado de degeneración, pérdida de estriaciones y necrosis.
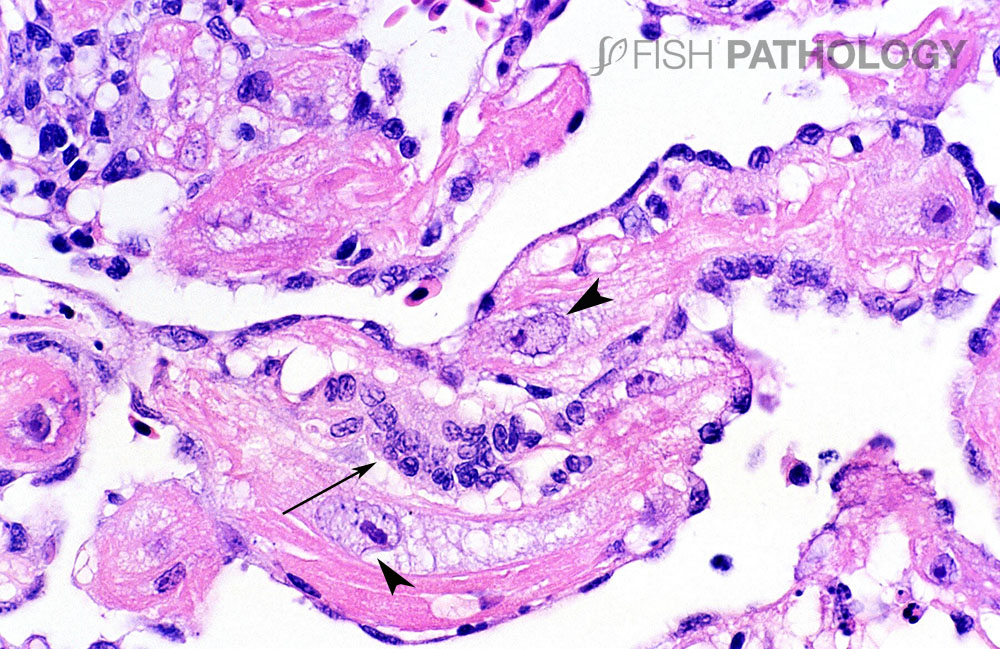
La fagocitosis que sigue del tejido necrótico conduce a “tubos” miocárdicos, en su mayoría huecos, llenos de células inflamatorias (mayormente monucleares), incluidos los macrófagos que eliminan residuos. En casos severos se pueden encontrar con frecuencia células similares a linfocitos en pericardio.
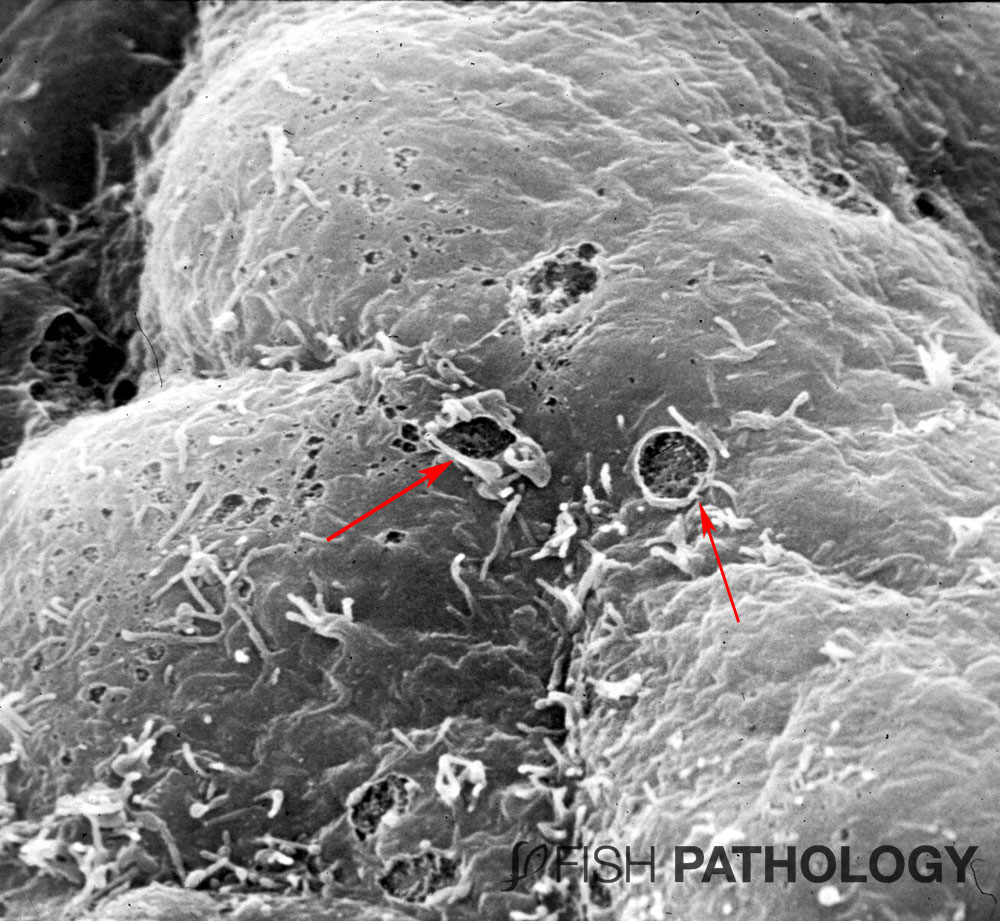
En etapas posteriores o avanzadas, la degeneración que sigue se puede ver a menudo, en vista de la compensación y regeneración del miocardio.
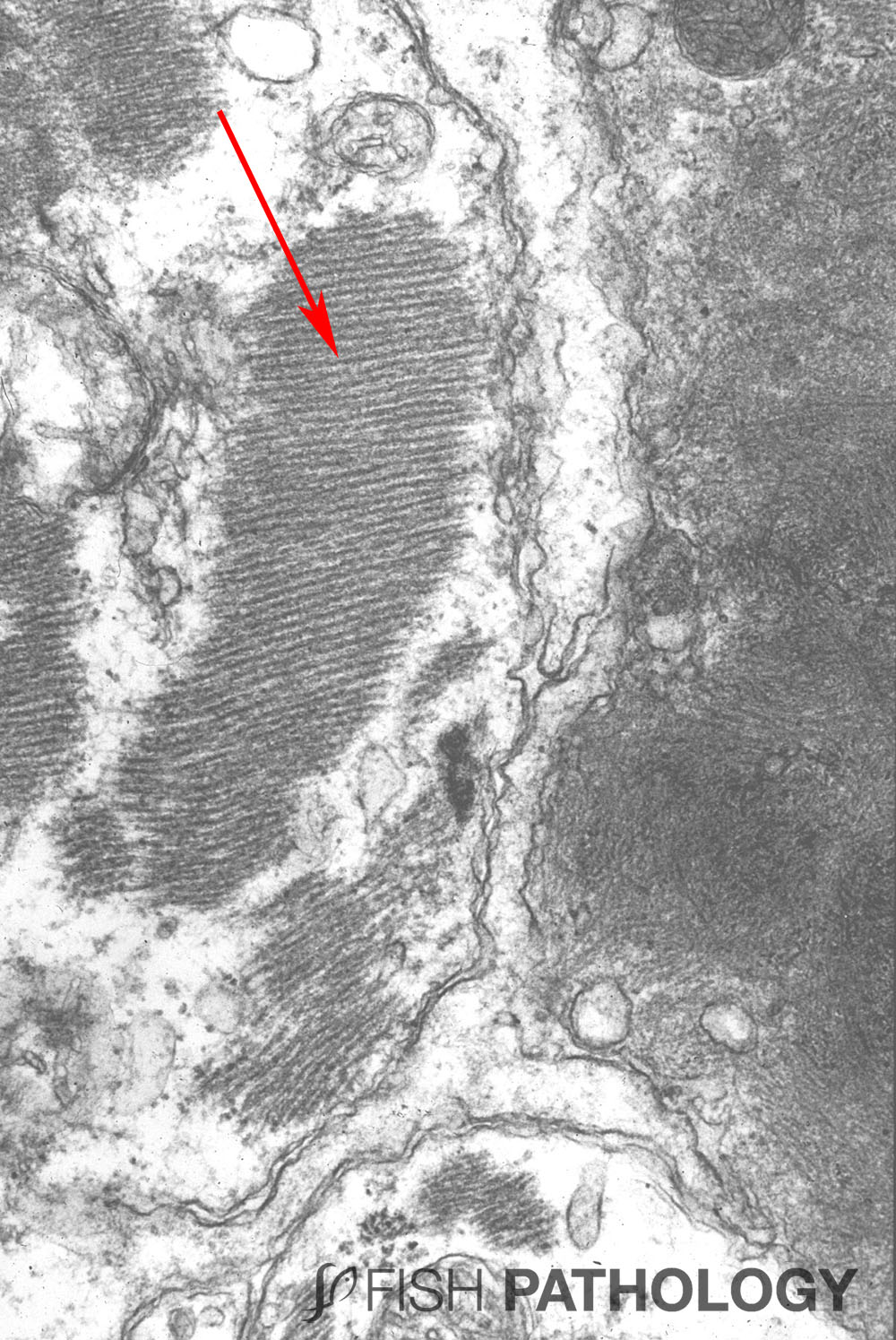
Estos cambios incluyen hipertrofia nuclear de miocitos adyacentes a las células gravemente afectadas. Pero también, puede incluir grupos de 5-20 núcleos similares a miocitos, sugiriendo el equivalente de “nuclear rowing” o “núcleos en fila o alineados” como se puede ver en la regeneración del músculo esquelético.
Las lesiones en hígado son típicas de “insuficiencia cardíaca hepática” con degeneración zonal de hepatocitos como consecuencia de la hipoxia.
REFERENCIAS
- Ferguson, H.W., T. Poppe, and D.J. Speare. (1990). Cardiomyopathy syndrome in farmed Norwegian salmon Salmo salar L. Dis. Aquat. Orgs. 8:225-231.
- Garseth, Å. H., Fritsvold, C., Svendsen, J.C., Bang Jensen, B. & Mikalsen, A.B. (2018). Cardiomyopathy syndrome in Atlantic salmon Salmo salar L.: A review of the current state of knowledge. J. Fish Diseases 41:11-26.
- Lovoll, M., Wiik‐Nielsen, J., Grove, S., Wiik‐Nielsen, C. R., Kristoffersen, A. B., Faller, R. & Tengs, T. (2010). A novel totivirus and piscine reovirus (PRV) in Atlantic salmon (Salmo salar) with cardiomyopathy syndrome (CMS). Virology Journal, 7, 309. https://doi.org/10.1186/1743-422X-7-309
- Wiik‐Nielsen, C. R., Ski, P. M. R., Aunsmo, A., & Lovoll, M. (2012). Prevalence of viral RNA from piscine reovirus and piscine myocarditis virus in Atlantic salmon, Salmo salar L., broodfish and progeny. J. Fish Diseases, 35, 169–171. https://doi.org/10.1111/j.1365-2761.2011.01328.x